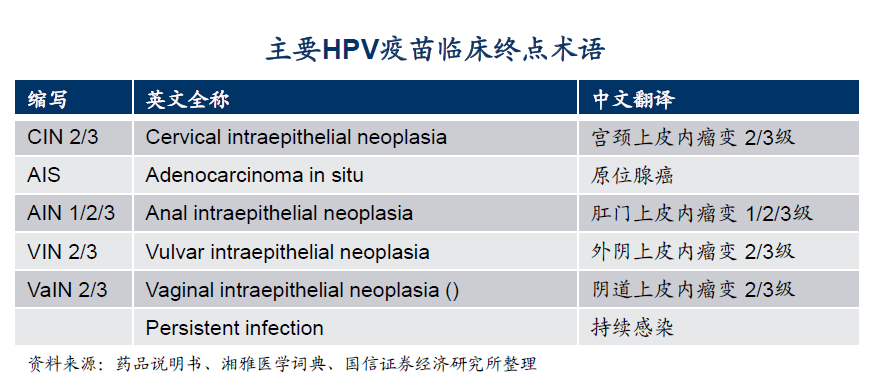
HPV疫苗延迟上市并非我国药审部门审批标准独特。2013年和2014年食药总局分别对GSK和默沙东的HPV上市申请给出了不批准的结论。一个流传的观点是CDE坚持采用WHO最早制定的宫颈上皮肉瘤病变(CIN2+)及以上作为临床试验终点指标,不认可欧美国家采用HPV持续病毒感染指标作为临床终点指标。实际上,虽然此后的日本和印度是采用的持续感染作为终点指标,但是美国的上市终点正是肉瘤病变,因此采用与原研获批的同样标准并非“歧视”。另一方面,FDA至今只批准了4种用于诊断HPV感染的试剂,而我国批准的该类试剂多达70余种,直到2015年国家器械审评中心2015年12月专门发布了《人乳头瘤病毒(HPV)核酸检测及基因分型、试剂技术审查指导原则》之后,我们对检测的准确性和灵敏度才有了一个更科学统一的基础,客观上也限制了临床以及审批的进度。
 海外产品上量与免疫规划渗透率挂钩。
海外产品上量与免疫规划渗透率挂钩。在美国HPV疫苗市场一直由本土企业默沙东把控,近两年来,产品销售增速已经逐渐稳定。从营收的增长来看,2011年到2016年增长了约10亿美元。根据美国CDC的估计,同期整体儿童的渗透率从30%上调至60%。美国一年大概出生400万儿童,因此30%儿童对应120万人,假设平均接种2剂,单剂价格在150美元,则对应增量3.6亿美元。除了美国本土的增长,全球其他地区纳入免疫规划或纳入国家财政支出,同样促进了HPV疫苗的放量。2017年一月,已经有65个国家将HPV纳入国家免疫规划之中。
 日本:曾经进入免疫规划,但退出出免疫规划后渗透率急降。
日本:曾经进入免疫规划,但退出出免疫规划后渗透率急降。日本在2010年将HPV疫苗免费提供给12~16岁的女生。但是在2013年因为一些不明原因的不良反应,自4月之后从国家免疫规划中剔除了。虽然HPV疫苗仍然属于财政支付的免费疫苗,但是仍然在在2014年出现了断崖式的下滑,渗透率迅速下降至近乎为零。2015年日本政府重申不会重新纳入免疫规划。日本宫颈癌筛查的渗透率长期以来一直持续在30%左右。HPV的较高价格仍然是接种的限制因素之一,在国家免费提供HPV疫苗之前,札幌的问卷调查中父母愿意给子女接种的意愿在1.5%左右,如果获得临床医生的推荐则会大幅提升接种意愿。在HPV疫苗进入国家免疫规划之前,20岁人群的HPV感染风险(16/18两种亚型)大概在1%左右,接种的数年中估计逐渐降低至0.3%左右。在14年及17年对医生的问卷调查中,支持将HPV纳入免疫规划的比例分别在61%和73.6%,有所提升,预计未来存在重新纳入免疫规划的可能。最近一个值得注意的动向是丹麦也出现了对默沙东HPV疫苗的疑惑,影响了后续的渗透率。
【免费下载】http://tinyurl.com/ybeewlmh
【备用下载】

 扫码加好友,拉您进群
扫码加好友,拉您进群